Сколько граммов оксида железа (II) нужно взять для взаимодействия с соляной кислотой, чтобы получить 2,54 г хлорида железа
РЕШЕНИЕ
FeO+2HCl=FeCl2+H2O
n(FeCl2)=m:M=2.54:127(56+35.5*2)= =0.02моль
m(FeO)=n*M=0.02*72(56+16)=1.44г
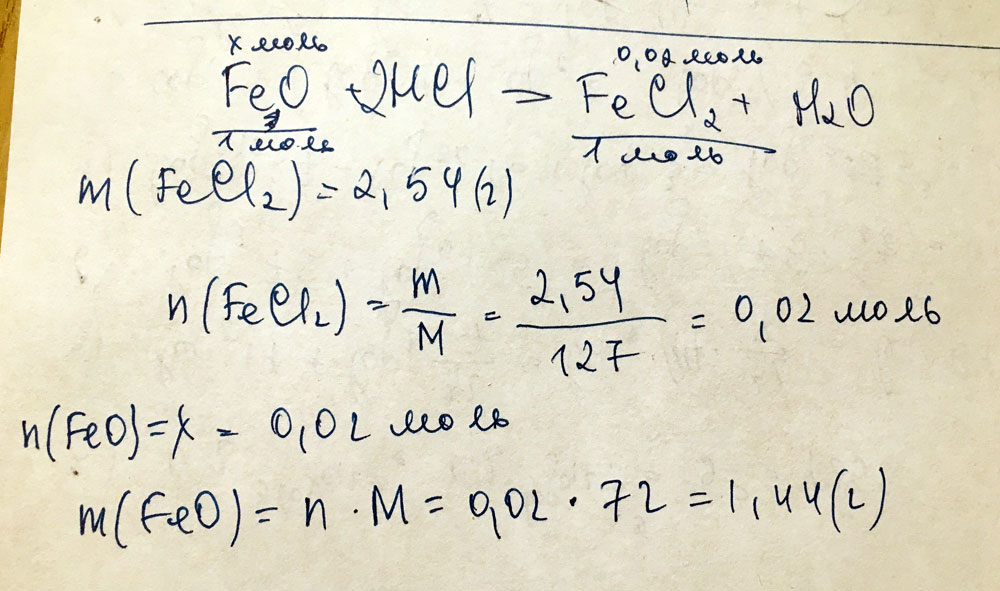
ПОХОЖИЕ ЗАДАНИЯ:
Тема: Что образуется после реакции
Тема: Сколько молей образуется при взаимодействии
Тема: Сколько молей образуется при взаимодействии
Тема: Оксиды
Тема: Оксиды