РЕШЕНИЕ
CO2+Ca(OH)2=CaCO3+H2O
Осадок это карбонат кальция, рассчитываем его молярную массу по ПС Менделеева=100
Для углекислого газа берем молярный объем газа при н, у=22,4
составляем пропорцию
5,6*100:22,4=25г
.
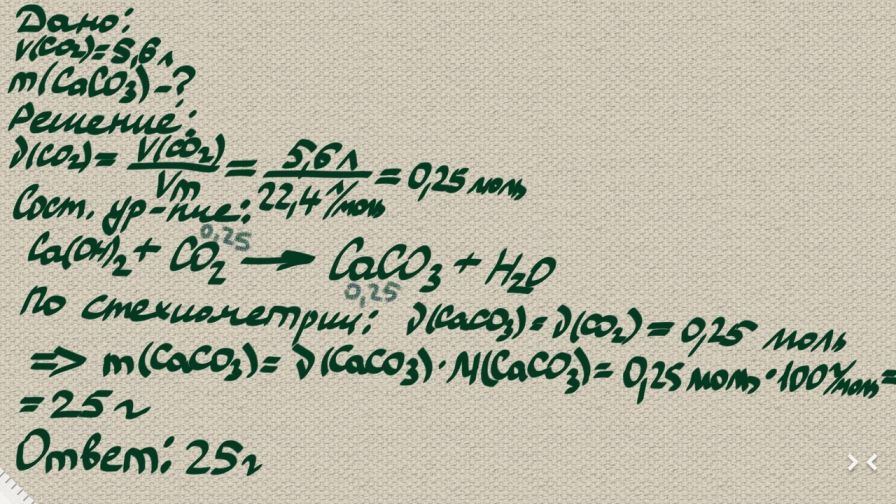
ПОХОЖИЕ ЗАДАНИЯ:
Тема: Определите массу и объем
Тема: Определите массу и объем
Тема: Какой объем кислоты
Тема: Какая масса соли образуется при взаимодействии
Тема: Вычислите массу осадка