Сколько г хлорида железа (III) получится при взаимодействии 280 г железа, содержащего 20% примесей, с хлором, если выход продукта реакции составляет 90% от теоретически возможного?
РЕШЕНИЕ
2Fe+3Cl2->2FeCl3
n(Fe)=m(Fe)/M(Fe)=280г*0,8/56г/моль=4 моль
n(FeCl3)=4 моль
m(FeCl3)=n(FeCl3)*M(FeCl3)=4моль*162,5г/моль=650 г
m’(FeCl3)=m(FeCl3)*r=650г*0,9=585 г
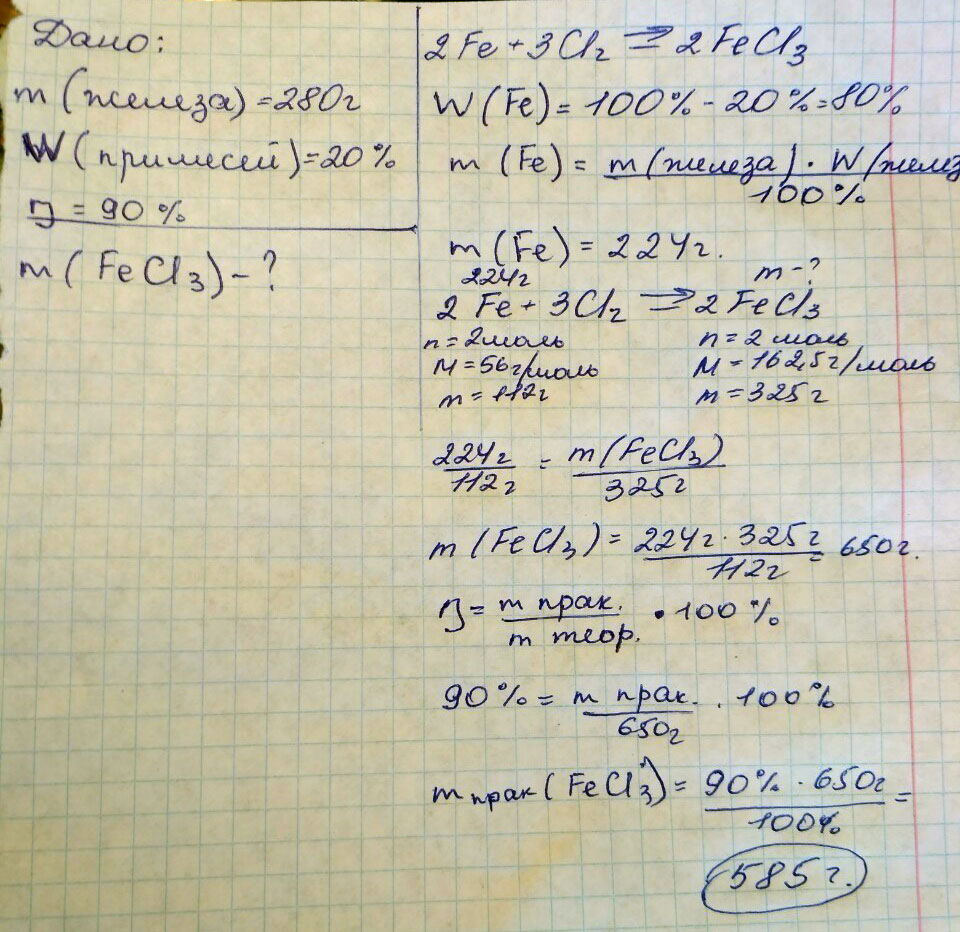
ПОХОЖИЕ ЗАДАНИЯ:
Тема: Вычислите массу осадка
Тема: Какая масса может быть получена
Тема: Оксиды
Тема: Какая масса соли образуется при взаимодействии
Тема: Оксиды